鋰 (Li)
银白色固体
![元素[鋰(Li)]](/element/element-7dc3fd4013618bbfcddbf1aeef23e3a6.jpg) 金属锂浮在煤油上
金属锂浮在煤油上
![元素[鋰(Li)]](/element/element-7dc3fd4013618bbfcddbf1aeef23e3a6.jpg) 金属锂浮在煤油上
金属锂浮在煤油上
基本資訊
| 原子序數 | 3 | 英文名 | Lithium |
|---|---|---|---|
| 所屬分類 | 碱金属 | 原子量 | 6.94 u |
| 熔點 | 180.54 °C | 沸點 | 1342 °C |
| 能級 | 2, 1 | 電負性 | 0.98 |
| 電子親和能 | 59.6 kJ/mol | 半徑(計算法) | 167 pm |
| 電離能 |
第1电离能: 520.2 kJ/mol
第2电离能: 7298.1 kJ/mol
第3电离能: 11815.0 kJ/mol
|
||
| 密度(常規) | 535 kg/m³ | 硬度(布式) | N/A |
| 體積模量 | 11 GPa | 導熱率 | 85 W/mK |
| 宇宙存量百分比 | 6.0E-7 % | ||
鋰,一種化學元素,其化學符號為Li,原子序數為3,呈現銀白色金屬外觀。 鋰因其在常溫下的低密度、低熔點特性以及卓越的電導性和熱導性而備受矚目,尤其值得注意的是,鋰能夠與水反應生成氫氣,並能與氧氣發生燃燒反應。 作為最輕的金屬之一,鋰的應用範圍廣泛且重要。 首要用途是在電池領域,尤其是鋰離子電池,它們被廣泛應用於便攜式電子設備(例如手機、筆記型電腦)和電動車輛等現代科技產品。 此外,鋰也用作合金成分以提升金屬的強度和韌性,常見於太空船和飛機零件的製造。 同時,鋰的化合物在藥物和陶瓷工業等領域也扮演關鍵角色。 在取得鋰資源方面,主要透過從含鋰礦石如莫洛礦和斑脈石中進行提取,主要採用化學處理方式將鋰從礦石中分離出來。 然而,儘管鋰具有許多優點,但在處理過程中需格外謹慎。 鋰易燃且能與水劇烈反應生成氫氣,因此必須避免其接觸濕氣或水分。 另外,鋰離子電池在特定條件下可能引發過熱和短路現象,這就要求我們在使用和儲存鋰電池時採取必要的安全措施。 尤其是在電池受損或處理不當的情況下,有可能導致有害物質洩漏,因此,正確處置和回收鋰電池顯得特別重要。 最後強調,以上資訊僅供參考,實際操作時務必嚴格遵循生產商提供的安全指南和操作建議,並確保充分理解並遵守當地的安全法規。
更多資訊
| 標準原子質量 | 6.941(2) |
|---|---|
| 電子排布 | 1s2 2s1 2, 1 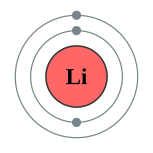 |
| 發現 | 約翰·奧古斯特·阿韋德松(1817年) |
| 分離 | 威廉·托馬斯·布蘭德(1821年) |
| 命名 | 永斯·貝吉里斯 |
| 物態 | 固態 |
| 密度 | (接近室溫) 0.534 g·cm−3 |
| 臨界點 | (估計) 3223 K,67 MPa |
| 熔化熱 | 3.00 kJ·mol−1 |
| 汽化熱 | 147.1 kJ·mol−1 |
| 比熱容 | 24.860 J·mol−1·K−1 |
| 氧化態 | +1, -1 (強鹼性氧化物) |
| 電負性 | 0.98(鮑林標度) |
| 原子半徑 | 152 pm |
| 共價半徑 | 128±7 pm |
| 范德華半徑 | 182 pm |
| 晶體結構 | 體心立方 |
| 磁序 | 順磁性 |
| 電阻率 | (20 °C)92.8 n Ω·m |
| 膨脹系數 | (25 °C)46 µm·m−1·K−1 |
| 聲速(細棒) | (20 °C)6000 m·s−1 |
| 楊氏模量 | 4.9 GPa |
| 剪切模量 | 4.2 GPa |
| 體積模量 | 11 GPa |
| 莫氏硬度 | 0.6 |
| CAS號 | 7439-93-2 |
元素清單
1號元素-氫(H)
2號元素-氦(He)
3號元素-鋰(Li)
4號元素-鈹(Be)
5號元素-硼(B)
6號元素-碳(C)
7號元素-氮(N)
8號元素-氧(O)
9號元素-氟(F)
10號元素-氖(Ne)
11號元素-鈉(Na)
12號元素-鎂(Mg)
13號元素-鋁(Al)
14號元素-矽(Si)
15號元素-磷(P)
16號元素-硫(S)
17號元素-氯(Cl)
18號元素-氬(Ar)
19號元素-鉀(K)
20號元素-鈣(Ca)
21號元素-鈧(Sc)
22號元素-鈦(Ti)
23號元素-釩(V)
24號元素-鉻(Cr)
25號元素-錳(Mn)
26號元素-鐵(Fe)
27號元素-鈷(Co)
28號元素-鎳(Ni)
29號元素-銅(Cu)
30號元素-鋅(Zn)
31號元素-鎵(Ga)
32號元素-鍺(Ge)
33號元素-砷(As)
34號元素-硒(Se)
35號元素-溴(Br)
36號元素-氪(Kr)
37號元素-銣(Rb)
38號元素-鍶(Sr)
39號元素-釔(Y)
40號元素-鋯(Zr)
41號元素-鈮(Nb)
42號元素-鉬(Mo)
43號元素-鍀(Tc)
44號元素-釕(Ru)
45號元素-銠(Rh)
46號元素-鈀(Pd)
47號元素-銀(Ag)
48號元素-鎘(Cd)
49號元素-銦(In)
50號元素-錫(Sn)
51號元素-銻(Sb)
52號元素-碲(Te)
53號元素-碘(I)
54號元素-氙(Xe)
55號元素-銫(Cs)
56號元素-鋇(Ba)
57號元素-鑭(La)
58號元素-鈰(Ce)
59號元素-鐠(Pr)
60號元素-釹(Nd)
61號元素-鉕(Pm)
62號元素-釤(Sm)
63號元素-銪(Eu)
64號元素-釓(Gd)
65號元素-鋱(Tb)
66號元素-鏑(Dy)
67號元素-钬(Ho)
68號元素-鉺(Er)
69號元素-銩(Tm)
70號元素-鐿(Yb)
71號元素-鑥(Lu)
72號元素-鉿(Hf)
73號元素-鉭(Ta)
74號元素-鎢(W)
75號元素-錸(Re)
76號元素-鋨(Os)
77號元素-銥(Ir)
78號元素-鉑(Pt)
79號元素-金(Au)
80號元素-汞(Hg)
81號元素-鉈(Tl)
82號元素-鉛(Pb)
83號元素-鉍(Bi)
84號元素-釙(Po)
85號元素-砹(At)
86號元素-氡(Rn)
87號元素-鈁(Fr)
88號元素-鐳(Ra)
89號元素-錒(Ac)
90號元素-釷(Th)
91號元素-鏷(Pa)
92號元素-鈾(U)
93號元素-鎿(Np)
94號元素-鈈(Pu)
95號元素-鎇(Am)
96號元素-鋦(Cm)
97號元素-錇(Bk)
98號元素-鐦(Cf)
99號元素-鎄(Es)
100號元素-鐨(Fm)
101號元素-鍆(Md)
102號元素-鍩(No)
103號元素-鐒(Lr)
104號元素-鑪(Rf)
105號元素-𨧀(Db)
106號元素-𨭎(Sg)
107號元素-𨨏(Bh)
108號元素-𨭆(Hs)
109號元素-䥑(Mt)
110號元素-鐽(Ds)
111號元素-錀(Rg)
112號元素-鎶(Cn)
113號元素-鉨(Nh)
114號元素-鈇(Fl)
115號元素-鏌(Mc)
116號元素-鉝(Lv)
117號元素-鿬(Ts)
118號元素-鿫(Og)