锘 (No)
| 原子序数 | 102 | 英文名 | Nobelium |
|---|---|---|---|
| 所属分类 | 锕系元素 | 原子量 | 259 u |
| 熔点 | 830 °C | 沸点 | 0 °C |
| 能级 | 2, 8, 18, 32, 32, 8, 2 | 电负性 | 1.3 |
| 电子亲和能 | N/A kJ/mol | 半径(计算法) | N/A pm |
| 电离能 |
第1电离能: 642 kJ/mol
第2电离能: 1254 kJ/mol
第3电离能: 2643 kJ/mol
第4电离能: 3956 kJ/mol
|
||
| 密度(常规) | N/A | 硬度(布式) | N/A |
| 体积模量 | N/A | 导热率 | N/A |
| 宇宙存量百分比 | 0 % | ||
锘(化学符号No,原子序数102)是一种人工合成的极高放射性金属元素,属于锕系元素,是第十个超铀元素,也是倒数第二个锕系成员。其寿命最长的同位素为锘-259,半衰期仅为58分钟,而在化学实验中最常用的是相对较易获得的锘-255,其半衰期为3.52分钟。由于锘的所有同位素半衰期短暂且无法通过中子捕获生成,它仅能在粒子加速器中通过粒子撞击轻元素来合成。鉴于生产困难及其短寿性质,锘目前除基础科学研究之外并无实际应用。 化学实验揭示了锘在元素周期表中与镱相似,表现出较重同类物的特性,尤其是在水溶液中的化学行为。与众不同的是,锘在水溶液中以+2氧化态较为稳定和常见,不同于大多数重锕系元素倾向于+3氧化态,这一特征符合早期科学家的预测。锘是镧系和锕系元素中独一无二的,其最稳定且最常见的氧化态为+2。 锘的命名是为了纪念瑞典著名科学家和炸药发明者阿佛烈·诺贝尔。在1950至1960年代期间,关于锘的发现存在多国实验室之间的争议,最终国际纯化学和应用化学联合会(IUPAC)在1997年正式承认前苏联的研究团队为锘的发现者,但仍保留了源自瑞典的“诺贝尔”这一名称。 在物理性质方面,锘展现出银白色金属光泽,具有良好的延展性、可塑性和导电性能,其熔点约1535℃,密度大约为7.87 g/cm³,在常温下表现出铁磁性。然而,上述关于锘的物理性质和用途描述并不准确,因为实际上,由于锘的极端不稳定性和放射性,这些常规金属特性和工业用途并未在现实世界中实现。 对于安全处理方面,尽管真实的锘元素不可能如普通金属那样被广泛应用,但如果处理此类放射性元素,必须格外谨慎。理论上,若接触高浓度的锘粉尘或气体,可能会对呼吸系统、眼睛和皮肤产生刺激。在实验室条件下处理类似放射性物质时,必须遵守严格的防护措施,穿戴个人防护装备,避免接近火源和氧化剂,并按照相关环保法规正确处置放射性废物。实际上,有关锘的安全信息更多关注其放射性危害的防范而非传统意义上的毒性或物理化学风险。
| 电子排布 | [Rn] 5f14 7s2 2, 8, 18, 32, 32, 8, 2 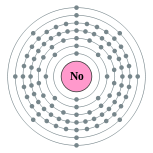 |
|---|---|
| 发现 | 杜布纳联合原子核研究所(1966年) |
| 物态 | 固体(预测) |
| 氧化态 | 2, 3 |
| 电负性 | 1.3(鲍林标度) |
元素列表