鑥 (Lu)
![元素[鑥(Lu)]](/element/element-aba01aa65d2ca0a0a602d56e809dd55f.jpg)
| 原子序數 | 71 | 英文名 | Lutetium |
|---|---|---|---|
| 所屬分類 | 镧系元素 | 原子量 | 174.967 u |
| 熔點 | 1663 °C | 沸點 | 3402 °C |
| 能級 | 2, 8, 18, 32, 9, 2 | 電負性 | 1.27 |
| 電子親和能 | 50 kJ/mol | 半徑(計算法) | 217 pm |
| 電離能 |
第1电离能: 523.5 kJ/mol
第2电离能: 1340 kJ/mol
第3电离能: 2022.3 kJ/mol
第4电离能: 4370 kJ/mol
第5电离能: 6445 kJ/mol
|
||
| 密度(常規) | 9841 kg/m³ | 硬度(布式) | 893 MPa |
| 體積模量 | 48 GPa | 導熱率 | 16 W/mK |
| 宇宙存量百分比 | 1.00E-8 % | ||
镥,作為一種稀土金屬元素,其化學符號標識為Lu,其單質呈現出典型的銀白色金屬光澤。 镥在稀土元素系列中獨樹一幟,擁有最硬且最密實的特性;其熔點高達1663攝氏度,沸點則為3395攝氏度,密度為9.8404g/cm³。 在常溫下,镥在空氣中表現出較好的穩定性,僅在一定條件下氧化為無色結晶體,並能溶於酸形成對應的無色鹽類。 在實際應用上,镥主要服務於研究工作,但也涉及其他特定用途,如它可溶於稀酸並與水發生緩慢反應,形成的鹽類呈現無色,而氧化物為白色。 自然界中存在的镥同位素主要包括穩定同位素175Lu和具有2.1×10^10年半衰期的β發射體176Lu。 由於自然界中镥儲量極為有限且提煉成本較高,故其價格較為昂貴。 镥通常透過使用鈣還原氟化镥LuF₃·2H₂O來獲取,並在原子能工業中有重要應用。 在不同的科技領域,镥發揮著至關重要的作用: 光學領域中,镥元素作為關鍵的光學材料,在光學玻璃、雷射和光纖通訊等方面展現突出價值。 在雷射製造中,镥憑藉其高效的雷射性能和較長的使用壽命,廣泛應用於雷射切割、雷射列印、雷射雕刻等技術。 而在光學玻璃中添加镥元素,能夠顯著提升玻璃的抗磨損和耐腐蝕性能,進而增強光學元件的耐用性和穩定性。 在醫療領域裡,镥元素被開發利用成為放射性藥物的核心成分,有效用於癌症及甲狀腺疾病的治療方案。 此外,镥還可合成醫用放射性標記劑,協助醫學影像診斷與標靶治療的進步。 在電子工業領域內,镥同樣具有重要作用,它可以作為電子裝置原料,被用來製造高品質的電容器、電感器和變壓器等核心元件。 不僅如此,镥元素在半導體材料範疇中有所貢獻,可用於生產高性能的電晶體、發光二極體等電子元件。
| 標準原子質量 | 174.9668(4) |
|---|---|
| 電子排布 | [氙] 4f14 5d1 6s2 2, 8, 18, 32, 9, 2 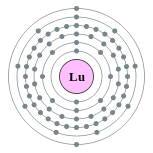 |
| 發現 | 喬治·於爾班和卡爾·奧爾·馮·威爾斯巴赫(1906年) |
| 分離 | 卡爾·奧爾·馮·威爾斯巴赫(1906年) |
| 物態 | 固體 |
| 密度 | (接近室溫) 9.841 g·cm−3 |
| 熔化熱 | ca. 22 kJ·mol−1 |
| 汽化熱 | 414 kJ·mol−1 |
| 比熱容 | 26.86 J·mol−1·K−1 |
| 氧化態 | 3, 2, 1 (弱鹼性氧化物) |
| 電負性 | 1.27(鮑林標度) |
| 原子半徑 | 174 pm |
| 共價半徑 | 187±8 pm |
| 晶體結構 | 六方密堆積 |
| 磁序 | 順磁性 |
| 電阻率 | (室溫)582 n Ω·m |
| 熱膨脹係數 | 室溫)9.9 µm/(m·K) |
| 楊氏模量 | 68.6 GPa |
| 剪切模量 | 27.2 GPa |
| 體積模量 | 47.6 GPa |
| 泊松比 | 0.261 |
| 維氏硬度 | 1160 MPa |
| 布氏硬度 | 893 MPa |
| CAS號 | 7439-94-3 |
元素清單